免疫細胞治療の歴史は1980年代のLAK療法に端を発しますが、当初は免疫細胞の種類も免疫応答の仕組みも解明が進んでおらず、正体が明らかでないキラーT細胞を増やすというもので、期待されるほどの効果は得られませんでした。しかしその後、CTL(細胞傷害性Tリンパ球)やDC(樹状細胞)の発見をはじめ、免疫細胞、がん細胞ともに分子レベルでの解明が進み、それに伴い免疫細胞治療もがん細胞またはそれに関連する因子に特異的に発現する分子を標的とする「分子標的治療」として進化、発展を遂げてきました。
がん治療における薬剤においても、1990年代からは分子標的薬がトレンドとなっていることはご存知の通りです。上皮成長因子受容体(EGFR)、血管内皮増殖因子(VEGF)、Her-2などを標的分子として作用する薬剤が次々に開発、承認されてきました。免疫細胞においても同様で、がん細胞上に特異的に発現する分子が同定され、それを標的として攻撃する免疫細胞とそれらの応答機構が明らかになっています。例えばCTLの標的分子は、がん細胞上の主要組織適合抗原(MHC)とそれに結合したがん抗原ペプチドであり、活性化されたアルファ・ベータT細胞、ガンマ・デルタT細胞、NK細胞などは、異常細胞に特有に発現するMIC A/Bをはじめとした複数の分子を標的とする、などです。このように、免疫細胞治療は、がん細胞上の分子を標的とした分子標的治療の一つといえるのです。
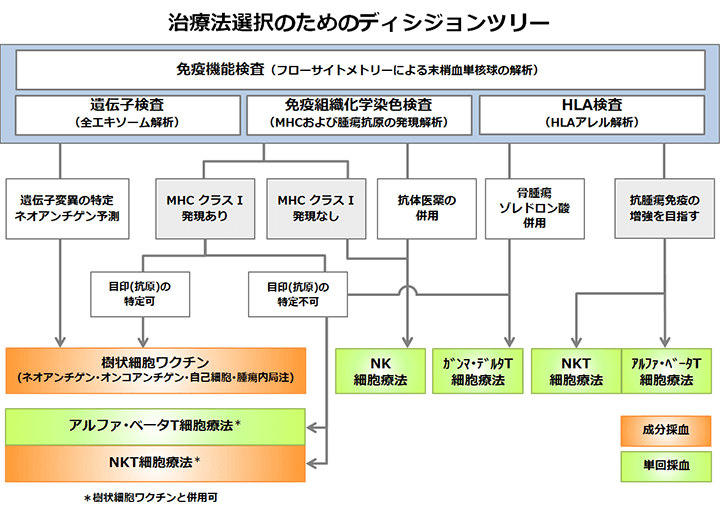
したがって、分子標的治療としての免疫細胞治療の有効性を引き出すには、標的とする分子が治療を受ける患者さんのがん細胞上の発現の程度を予め調べ、適応を判断することが重要です。すなわち治療の個別化です。分子標的薬においても、Her-2陽性の症例にハーセプチンが、EGFRに変異のある症例にはイレッサが奏効しやすいというのと同じです。
例えば先のMHCの発現は、約4割の患者さんのがん細胞で消失あるいは低下していることが当クリニックの統計で明らかになりました。これらの例ではCTLを誘導するDCワクチンの効果は期待が薄いということになります。当院では、「免疫組織化学染色検査」という方法を導入し、患者さんのがん細胞表面におけるMHCクラスⅠの発現を事前に確認したり、後述する樹状細胞ワクチンにおいて「人工抗原ペプチド」を用いる際には、患者さん自身に適合するかどうか確認するため「MHC組織適合検査」を行ったりなど、患者さん一人ひとりに最適な治療を、分子レベルで見極めて治療を行なっています。
また、抗体医薬を使用している場合は、がん細胞に結合した抗体医薬のFc領域という部分を標的としてガンマ・デルタT細胞療法等を併用することで、治療効果を高めることが期待できるなど、三大療法との併用による効果も明らかになりつつあります。そのため、患者さんの現在受けている治療、あるいは過去に受けた治療内容も、免疫細胞治療の個別化を行う上での重要な判断材料となります。

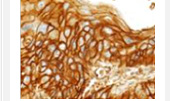
![[MHCクラスIが多いがん組織] 樹状細胞ワクチンなどの治療法が有効と考えられる](img/index_img04.png)
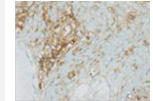
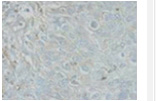
![[MHCクラスIが少ないがん組織] NK細胞療法、ガンマ・デルタT細胞療法、アルファ・ベータT細胞療法などの有効性が維持できる](img/index_img09.png)


